最新!3月重点医药政策盘点
发布时间:
2025年05月06日 阅读量:
410
一、本月国家部委发文政策收集统计
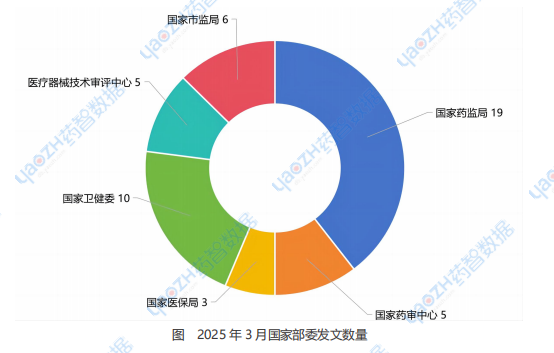
2025年3月�,�,,�,,药智网收集的国家药监局发文政策19条�;;;;;;�;�;国家药审中心发文政策5条�;;;;;;�;�;国家医保局发文政策3条�;;;;;;�;�;国家卫健委发文政策10条�;;;;;;�;�;医疗器械技术审评中心发文政策5条�;;;;;;�;�;国家市场监督管理局发文政策6条�。�。�。。�。�。�。�。
二、本月医药政策速览
药品类
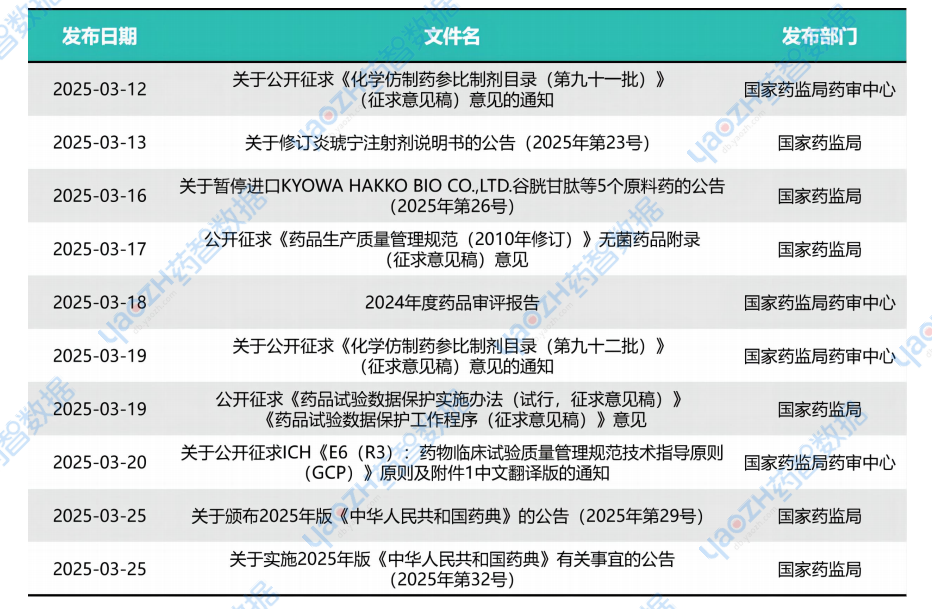
数据来源:药智数据-政策法规数据库
医疗器械类

数据来源:药智数据-政策法规数据库
其他类

数据来源:药智数据-政策法规数据库
药品类重点法规梳理:
1. 国家药监局综合司公开征求《药品生产质量管理规范(2010年修订)》无菌药品附录(征求意见稿)意见
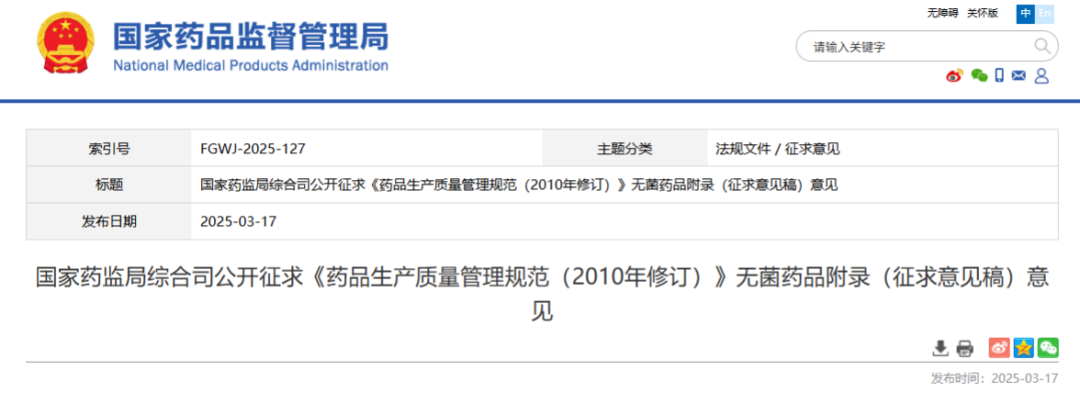
国家药监局近期发布的《药品生产质量管理规范(2010年修订)》无菌药品附录(征求意见稿)对现行规范进行了全面修订�,�,,�,,旨在提升无菌药品生产的质量安全水平�,�,,�,,并与国际标准接轨�。�。�。。�。�。�。�。以下是相较于现行版本(2011年版)的主要变化点:
(1)条款与术语全面扩充
条款增量:由81条跃升至235条�,�,,�,,细化要求更精准�。�。�。。�。�。�。�。
术语拓展:从6个增至33个�,�,,�,,新增“细菌截留试验”等关键术语�。�。�。。�。�。�。�。
(2)适用范围进一步拓宽
明确将无菌辅料及直接接触药品的无菌包装材料生产纳入规范�。�。�。。�。�。�。�。
(3)污染控制策略(CCS)全新引入
要求企业建立涵盖多方面的CCS�,�,,�,,并定期审核更新�,�,,�,,确保污染预防效果�。�。�。。�。�。�。�。
(4)洁净区与设施标准升级
分级细化:明确A级至D级洁净区风险等级�。�。�。。�。�。�。�。
技术革新:鼓励使用隔离器、RABS等先进技术�,�,,�,,减少人为干预�。�。�。。�。�。�。�。
气流研究:A级区需进行静态和动态气流深入研究�。�。�。。�。�。�。�。
(5)人员管理力度加强
A/B级区人员需定期无菌更衣确认及气流可视化培训�。�。�。。�。�。�。�。
减少洁净区人员数量�,�,,�,,规范操作行为�,�,,�,,确�;;;;;;�;�;肪澄榷�。�。�。。�。�。�。�。
(6)生产与灭菌管理细化升级
灭菌工艺优先:首选最终灭菌�,�,,�,,必要时采用除菌过滤并验证完整性�。�。�。。�。�。�。�。
技术管理细化:明确FFS、BFS等特定技术要求�。�。�。。�。�。�。�。
无菌工艺模拟:模拟最差条件�,�,,�,,验证无菌工艺有效性�。�。�。。�。�。�。�。
(7)质量控制与监测全面强化
环境监测数据成为批次放行重要依据�。�。�。。�。�。�。�。
鼓励采用已验证的自动化微生物检测方法�。�。�。。�。�。�。�。
无菌检查结合环境监测数据�,�,,�,,确保产品安全�。�。�。。�。�。�。�。
(8)包装容器密封性要求优化
熔封产品根据容量制定不同测试标准�。�。�。。�。�。�。�。
非熔封产品需基于风险评估制定抽样计划�。�。�。。�。�。�。�。
(9)5.0μm粒子标准调整
A级区不再强制要求静态和动态监测5.0μm粒子�,�,,�,,适应新标准�。�。�。。�。�。�。�。
(10)与国际标准接轨
参考欧盟GMP附录1(2022版)�,�,,�,,引入CCS、PUPSIT等国际概念�,�,,�,,推动规范国际化�。�。�。。�。�。�。�。
2. 国家药监局综合司公开征求《药品试验数据�;;;;;;�;�;な凳┌旆ǎㄊ孕�,�,,�,,征求意见稿)》《药品试验数据�;;;;;;�;�;すぷ鞒绦颍ㄕ髑笠饧澹芬饧

图片来源:NMPA官网
《药品试验数据�;;;;;;�;�;な凳┌旆ǎㄊ孕�,�,,�,,征求意见稿)》和《药品试验数据�;;;;;;�;�;すぷ鞒绦颍ㄕ髑笠饧澹返某鎏�,�,,�,,标志着我国药品试验数据�;;;;;;�;�;ぶ贫鹊恼浇�,�,,�,,这一制度的建立�,�,,�,,将为医药创新提供更加有力的法律保障�,�,,�,,促进医药行业的高质量发展�。�。�。。�。�。�。�。以下是两份征求意见稿的核心内容、创新点、实施机制及政策意义�。�。�。。�。�。�。�。
(1)核心内容
�;;;;;;�;�;ざ韵螅捍葱乱⒏牧夹托乱⒎轮埔┓掷啾�;;;;;;�;�;�,�,,�,,覆盖化药和生物药�。�。�。。�。�。�。�。
�;;;;;;�;�;て谙蓿
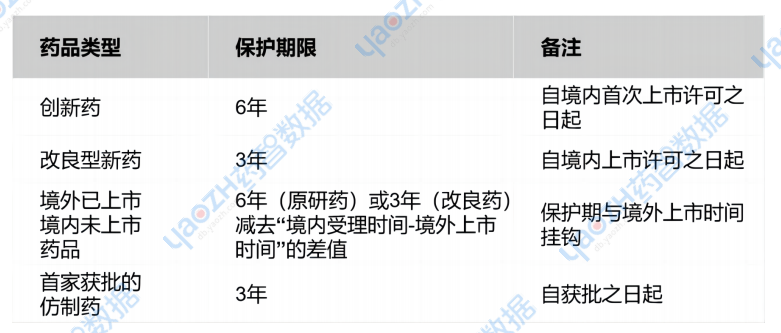
�;;;;;;�;�;し段В喊踩浴⒂行浴⒅柿渴荩ú缓珺E/免疫原性数据)�。�。�。。�。�。�。�。
(2)政策亮点
覆盖生物药:CAR-T、单抗等纳入�;;;;;;�;�;�。�。�。。�。�。�。�。
适应症独立�;;;;;;�;�;ぃ和灰┢凡煌视χ⒖煞直鹕昵�。�。�。。�。�。�。�。
鼓励全球同步:境外药品在华�;;;;;;�;�;て谟牒M馍鲜惺奔涔夜�。�。�。。�。�。�。�。
数据资产化:允许原研企业授权仿制药企使用数据�。�。�。。�。�。�。�。
(3)实施机制
申请公示:上市申请时同步提交�,�,,�,,CDE公示�;;;;;;�;�;ば畔�。�。�。。�。�。�。�。
�;;;;;;�;�;て谙拗疲悍轮埔┢笪淳砜梢览翟幸┦鼙�;;;;;;�;�;な菡卟挥枧�。�。�。。�。�。�。�。
终止情形:药品撤销或持有人放弃时�;;;;;;�;�;ぶ罩�。�。�。。�。�。�。�。
(4)政策意义
激励创新:数据独占弥补专利�;;;;;;�;�;げ蛔�。�。�。。�。�。�。�。
仿制平衡:允许�;;;;;;�;�;て诮崾1年提交仿制申请�。�。�。。�。�。�。�。
国际对标:参考美欧数据�;;;;;;�;�;つJ�,�,,�,,符合WTO规则�。�。�。。�。�。�。�。
3. 国家药监局 国家卫生健康委关于颁布2025年版《中华人民共和国药典》的公告(2025年第29号)、国家药监局关于实施2025年版《中华人民共和国药典》有关事宜的公告(2025年第32号)
图片来源:NMPA官网
2025年版《中华人民共和国药典》(以下简称《中国药典》)�,�,,�,,以及药典实施有关事宜的公告已由国家药监局、卫健委颁布�,�,,�,,自2025年10月1日起实施�。�。�。。�。�。�。�。
声明:本文观点仅代表作者本人�,�,,�,,不代表本网站立场�,�,,�,,欢迎在留言区交流补充�;;;;;;�;�;如需转载�,�,,�,,请务必注明文章作者和来源�。�。�。。�。�。�。�。如涉及作品内容、版权和其它问题�,�,,�,,请在本平台留言�,�,,�,,我们将在第一时间处理�。�。�。。�。�。�。�。
